口服减肥药大战打响.
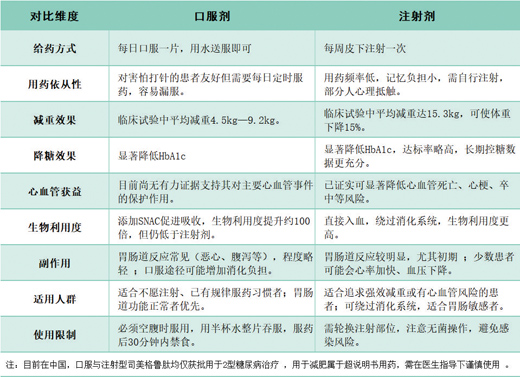
张力制表
2026年,减肥药赛道早已告别诺和诺德一家独大的旧格局。随着司美格鲁肽核心化合物专利到期,国内市场迎来全新竞争态势:信达生物玛仕度肽注射液III期临床试验成功达成主要终点,来凯医药、先为达生物等本土企业则加速冲刺港股IPO,试图在资本与市场的双重赛道抢占先机。
进入4月份,口服剂型的商业化落地,成为全球减肥药赛道的新焦点。4月1日,礼来旗下口服小分子GLP-1(胰高血糖素样肽-1)受体激动剂orforglipron(商品名Foundayo)获美国食品药品监督管理局(FDA)批准上市,用于成人肥胖或超重治疗。这是全球首款获批的口服小分子非肽类GLP-1受体激动剂,目前,礼来正推进该产品在中国市场的上市申请,有望进一步搅动国内减重市场。
事实上,口服GLP-1药物的商业化竞赛早已开启。今年1月5日,诺和诺德宣布口服版Wegovy在美国正式上市。这款产品早在2025年12月22日就已获得FDA批准,用于肥胖或超重成人的长期体重管理,是美国首款获批的口服GLP-1减重药物,其上市标志着减肥药正式迈入口服时代。
国产口服剂型取得进展
当前,国内减肥药市场已呈现原研药、国产创新药与仿制药全面混战的格局,而令人欣喜的是,不少本土企业已在人工合成的口服小分子化合物GLP-1激动剂领域取得突破性进展。比如,华东医药、恒瑞医药、海思科、一品红、信立泰、闻泰科技等一众企业纷纷入局,加速布局这一潜力赛道。
其中,闻泰科技的进展尤为引人注目。该公司正计划赴港上市,其核心资产为口服小分子GLP-1受体激动剂CX11,拟募资规模约1亿美元至2亿美元。CX11目前在国内已顺利完成II期临床试验,展现出“具有竞争力的减重效果”,并于2024年年底启动了III期注册性临床试验。在美国,CX11也同步开展针对肥胖及超重患者的II期临床试验,推进其全球临床布局。
CX11之所以能在众多管线中脱颖而出,源于2024年12月的一笔重要交易。箕星药业收购了CX11在中国以外市场的全球独家开发和商业化权益。紧接着,2026年1月,箕星药业成功完成2.87亿美元D1轮融资,由SR One、TCGX、RA Capital等全球顶级医疗基金联合投资,箕星药业明确表示,将把资金用于CX11的全球临床开发,这无疑为CX11的未来发展注入了强大动力。
在研发进展方面,华东医药的HDM1002和恒瑞医药的HRS-7535目前已进入III期临床试验阶段,海思科等企业的相关项目也在持续稳步推进。
海外授权合作频繁
回顾近年来的交易动态,国产GLP-1药物的海外授权合作频繁且成果显著。2023年11月,诚益生物将AZD5004海外权益授权给阿斯利康,获得首付款1.85亿美元及后续最高18.25亿美元的里程碑款项;2024年5月,恒瑞医药将HRS-7535、HRS-9531和HRS-4729三款GLP-1系列产品的海外权益,以1亿美元首付款、最高59.25亿美元里程碑款项的价格授权给与贝恩资本合资成立的子公司;2024年12月,翰森制药将临床前口服GLP-1小分子HS-10535全球权益授权给默沙东;2025年12月,复星医药旗下的药友制药将其口服小分子GLP-1受体激动剂YP05002的海外权益授权给辉瑞。这些交易不仅体现了国产GLP-1药物的研发实力,也为企业带来了丰厚的资金回报和全球化发展机遇。
然而,国产口服GLP-1药物的发展之路也面临着诸多现实压力。国际制药巨头在该领域的竞争优势明显,礼来的口服小分子GLP-1受体激动剂orforglipron已获得FDA批准上市,诺和诺德的口服减重产品也已成功上市,罗氏、阿斯利康、默沙东等跨国企业手中也拥有各自的后备项目,它们凭借强大的研发实力、丰富的临床经验和广泛的市场渠道,对国产口服药构成了巨大的竞争压力。
业内认为,随着竞争加剧,市场对减肥药的评价标准也在不断提高。减重幅度不再是唯一的衡量标准,胃肠道反应、停药率、是否需要空腹、给药频率以及定价空间等因素,都会直接影响产品在市场中的竞争力和地位。如果国内项目长期停留在Fast Follow(快速跟随的模仿式创新)阶段,缺乏自主创新和差异化优势,未来很可能会面临更加激烈的价格竞争和拥挤的临床研发环境。
MNC在卷什么
诺和诺德和礼来在2026年先后把口服产品推向市场,但两家走的是两条不同路线。前者是将成熟分子口服化,后者则是用小分子重新开发GLP-1口服药。这两条路径几乎同时走到商业化阶段,也让口服GLP-1的竞争格局一下子清晰起来。
诺和诺德的Wegovy口服片(semaglutide 25mg)是一种多肽,结构上与人体自然分泌的GLP-1激素相似。多肽容易被胃酸消化,所以注射用的semaglutide生物利用度约89%;但做成口服就比较麻烦,必须借助一种名叫SNAC的吸收促进剂在胃里“护送”它穿过胃壁,进入血液的比例仅约1%。这就是为什么同样是 semaglutide,口服片要早起空腹服药,且只能用不超过4盎司(约120ml)的水送服,还要等至少30分钟才能再吃东西。
礼来的口服剂Foundayo(orforglipron)则是小分子,不是多肽,不怕胃酸,可直接在小肠被动吸收。orforglipron的口服生物利用度达到20%—40%,不需要吸收促进剂和空腹限制。一项更新的研究甚至报告其利用度接近79%。这大约是诺和诺德口服剂semaglutide的80倍。
同样是口服剂型,到底谁减得多?礼来的Foundayo在ATTAIN-1三期试验中,72周时三种剂量均达到主要终点,36mg最高剂量组平均减重12.4%(27.3磅)。
诺和诺德Wegovy口服片的OASIS 4三期试验显示,64周时平均减重13.6%,但样本量仅307人(非糖尿病患者)。完全依从服药要求的参与者减重达16.6%,其中约三分之一减重超过20%。
不过,诺和诺德Wegovy口服剂型的OASIS 4试验样本量只有307人,礼来的Foundayo在ATTAIN-1试验阶段则有4500多人;且双方试验的持续时间也不相同,礼来用时72周,而诺和诺德用时64周。目前还无法对比确切的减重数量。
值得注意的是,两款口服剂型药品的副作用几乎一致:恶心、呕吐、腹泻、便秘……这是整个GLP-1类药物的共性,也是药物在放慢胃排空、抑制食欲时的“副产品”,通常在加药初期最明显,之后逐渐减轻。
不过,在停药率、肝毒性和心血管获益以及甲状腺肿瘤副作用方面,两款药有略微不同。礼来的Foundayo和诺和诺德的Wegovy口服片均含有针对甲状腺C细胞肿瘤的黑框警告,有甲状腺髓样癌个人或家族史或多发性内分泌腺瘤病2型的患者禁用。这是GLP-1类的共性警示,由动物实验观察得到,人类面临的实际风险尚不明确。
肝毒性是所有小分子药物的“原罪担忧”,因为小分子药物必须经肝脏代谢,理论上有肝损伤风险。好消息是,礼来的Foundayo在研究中均未发现肝脏异常信号。而诺和诺德的Wegovy口服片在停药率方面可能略胜一筹。
(文章来源:国际金融报)
声明:
- 风险提示:以上内容仅来自互联网,文中内容或观点仅作为原作者或者原网站的观点,不代表本站的任何立场,不构成与本站相关的任何投资建议。在作出任何投资决定前,投资者应根据自身情况考虑投资产品相关的风险因素,并于需要时咨询专业投资顾问意见。本站竭力但不能证实上述内容的真实性、准确性和原创性,对此本站不做任何保证和承诺。
- 本站认真尊重知识产权及您的合法权益,如发现本站内容或相关标识侵犯了您的权益,请您与我们联系删除。









推荐文章: